Фосфоресценција је луминисценција која се јавља када енергије испоручује електромагнетно зрачење, обично ултраљубичасто светло. Извор енергије удара електрон ан атом из стања ниже енергије у „узбуђено“ више енергетско стање; онда електрон ослобађа енергију у облику видљива светлост (луминисценција) када се врати у стање ниже енергије.
Кључни поступци: фосфоресценција
- Фосфоресценција је врста фотолуминисценције.
- У фосфоресценцији светлост апсорбује материјал, надувајући енергетске нивое електрона у побуђено стање. Међутим, енергија светлости не одговара сасвим енергији дозвољених побуђених стања, па се апсорбоване фотографије заглаве у троструком стању. Прелази у ниже и стабилније енергетско стање изискује време, али када се појаве, светлост се ослобађа. Пошто се ово ослобађање одвија полако, изгледа да фосфоресцентни материјал светли у мраку.
- Примери фосфоресцентних материјала укључују сјаје у мраку, неке сигурносне знакове и ужарену боју. За разлику од фосфоресцентних производа, флуоресцентни пигменти престају да светлују након што се уклони извор светлости.
- Иако је назван по зеленом сјају елемента фосфор, фосфор заправо светли због оксидације. Није фосфоресцентна!
Једноставно објашњење
Фосфоресцентност полако ослобађа складиштену енергију током времена. У основи, фосфоресцентни материјал се "пуни" излагањем светлости. Тада се енергија складишти током одређеног времена и полако се ослобађа. Када се енергија ослобађа одмах након апсорбирања енергије која се појављује, поступак се позива флуоресценција.
Објашњење квантне механике
У флуоресценцији, површина апсорбује и поново емитује фотон готово тренутно (око 10 наносекунди). Фотолуминисценција је брза јер енергија апсорбованих фотона одговара енергетским стањима и дозвољеним прелазима материјала. Фосфоресценција траје много дуже (милисекунде до дана), јер апсорбовани електрон прелази у побуђено стање са већом множином спина. Узбуђени електрони бивају заробљени у троструком стању и могу само да користе „забрањене“ прелазе да би се спустили у ниже енергетско синглетно стање. Квантна механика омогућава забрањени прелаз, али они нису кинетички повољни, па им треба дуже време. Ако се апсорбује довољно светлости, ускладиштена и ослобођена светлост постаје довољно значајна да би материјал могао да "светлуца у тамно. "Из тог разлога, фосфоресцентни материјали, попут флуоресцентних материјала, изгледају врло светли под црном (ултраљубичастом) светлошћу. Јаблонски дијаграм се обично користи за приказ разлике између флуоресценције и фосфоресценције.
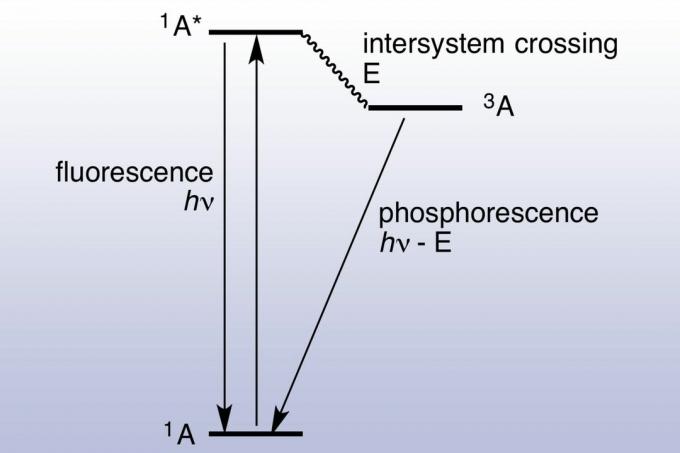
Историја
Проучавање фосфоресцентних материјала датира бар из 1602. године када је Италијан Винцензо Цасциароло описао „лапис соларис“ (сунчани камен) или „лапис лунарис“ (месечев камен). Откриће је описано у књизи професора филозофије Гиулио Цесаре ла Галла из 1612. године Де Пхеноменис у Орбе Лунае. Ла Галла извјештава да је Цасциароло камен пропустио свјетлост након што се калцифицирао загријавањем. Добијала је светлост од Сунца и тада је (попут Месеца) у тами испуштала светлост. Камен је био нечист барит, мада и други минерали показују фосфоресценцију. Они укључују неке дијаманти (познат индијском краљу Бхоји још 1010-1055. године, поново га је открио Албертус Магнус и поново га је открио Роберт Боиле) и бели топаз. Кинези су, посебно, ценили врсту флуорита званог хлорофан који би приказивао луминисценцију од телесне топлоте, излагања светлости или трљања. Интересовање за природу фосфоресценције и друге врсте луминисценције на крају је довело до открића радиоактивности 1896. године.
Материјали
Поред неколико природних минерала, фосфоресценција се производи и хемијским једињењима. Вероватно најпознатији од њих је цинк сулфид, који се у производима користи од 1930-их. Цинк сулфид обично емитује зелену фосфоресценцију, мада се фосфори могу додати да промене боју светлости. Фосфор апсорбује светлост коју емитује фосфоресценција и потом је ослобађа као другу боју.
У новије време стронцијум-алуминат се користи за фосфоресценцију. Ово једињење светли десет пута сјајније од цинков сулфида и такође дуго чува своју енергију.
Примери фосфоресценције
Уобичајени примери фосфоресценције укључују звезде које људи постављају на зидове спаваће собе који светлују сатима након што се угасе светла и боје које се користе за прављење ужарених звезда фрески. Иако елемент фосфор светли зеленом бојом, светло се ослобађа од оксидације (хемилуминисценција) и јесте не пример фосфоресценције.
Извори
- Франз, Карл А.; Кехр, Волфганг Г.; Сиггел, Алфред; Виецзорецк, Јурген; Адам, Валдемар (2002). "Луминесцентни материјали" у Уллманнова енциклопедија индустријске хемије. Вилеи-ВЦХ. Веинхеим дои: 10.1002 / 14356007.а15_519
- Рода, Алдо (2010). Хемилуминисценција и биолуминисценција: прошлост, садашњост и будућност. Краљевско хемијско друштво.
- Зитоун, Д.; Бернауд, Л.; Мантегхетти, А. (2009). Микроталасна синтеза дуготрајног фосфора. Ј. Цхем. Едуц. 86. 72-75. дои: 10.1021 / ед086п72